Cuando un electrodo de metal entra en contacto con una solución electrolítica, ocurre algo que no tiene equivalente en ninguna otra parte de la química: el sistema entero, eso es iones, moléculas de disolvente, electrones del metal, se reorganiza espontáneamente para minimizar la energía en una región de apenas uno o dos nanómetros de grosor. Esa región organizada es la doble capa eléctrica, y entenderla no es un ejercicio académico: es la razón por la que los supercondensadores pueden cargarse en segundos, por la que los sensores de glucosa pueden medir concentraciones de micromolar, y por la que diseñar una batería de carga rápida es más difícil de lo que parece.
Este artículo explica qué es la doble capa, cómo está estructurada y por qué su física dicta el comportamiento de tecnologías que van desde el galvanizado industrial hasta los vehículos eléctricos.
Dos tipos de proceso, la misma interfaz
En cualquier electrodo sumergido en solución pueden ocurrir dos categorías de proceso completamente distintas.
- Los procesos faradaicos son los que la mayoría asocia con la electroquímica: electrones que cruzan físicamente la interfaz metal-solución, oxidando o reduciendo especies químicas. La cantidad de reacción es estrictamente proporcional a la carga que pasa. Eso es la ley de Faraday, y es la base del funcionamiento de baterías, pilas de combustible y procesos electrolíticos industriales.
- Los procesos no faradaicos no implican transferencia de carga a través de la interfaz. Sin embargo, la interfaz no está inactiva: las moléculas de disolvente se reorientan, los iones se acercan o se alejan, y la estructura de esa zona responde al potencial aplicado. Corrientes externas transitorias pueden fluir sin que ningún electrón cruce la frontera.
La distinción importa porque en cualquier experimento electroquímico real ambos procesos coexisten, y la corriente que se mide es la suma de ambas contribuciones. Separar una de la otra es uno de los retos prácticos centrales del diseño de sensores y baterías.
El electrodo polarizado ideal: un laboratorio mental útil
Para estudiar la estructura de la interfaz sin el ruido de las reacciones químicas, los electroquímicos trabajan con el concepto de electrodo polarizado ideal (IPE, del inglés ideal polarized electrode): un electrodo teórico en el que ninguna transferencia de carga puede ocurrir, independientemente del potencial aplicado.
Ningún electrodo real se comporta exactamente así, pero algunos sistemas se aproximan bastante en rangos de potencial acotados. El ejemplo clásico es un electrodo de mercurio en solución de cloruro de potasio desaireada: en una ventana de unos 2 V, la energía disponible no es suficiente para oxidar el mercurio ni para reducir los iones de potasio, de modo que la única corriente que fluye es no faradaica. Ese rango de potencial es la ventana experimental donde la doble capa puede estudiarse de forma relativamente limpia.
Dentro de esa ventana, el comportamiento de la interfaz es análogo al de un condensador eléctrico: la carga en el metal, igual y opuesta a la carga en la solución, separadas por una distancia de escala nanométrica. La capacitancia de doble capa que caracteriza la interfaz toma típicamente valores entre 10 y 40 µF/cm², varios órdenes de magnitud superiores a los condensadores convencionales de geometría comparable, precisamente porque la separación de carga es de dimensiones atómicas.
Anatomía de la doble capa
La solución no forma una pared rígida y estática frente al electrodo. Lo que existe es una estructura de capas con propiedades distintas, que la electroquímica moderna describe así:
La capa interna (o capa compacta de Helmholtz)
Es la región más próxima al electrodo. Contiene moléculas de disolvente orientadas por el campo eléctrico y, en muchos sistemas, iones que se adsorben directamente sobre la superficie metálica mediante interacciones químicas específicas: fuerzas de naturaleza covalente o cuasi-covalente, no meramente electrostáticas. A este fenómeno se lo llama adsorción específica, y tiene consecuencias prácticas concretas: un aditivo en un baño de galvanizado que se adsorbe específicamente puede, por ejemplo, cambiar radicalmente la morfología del depósito metálico.
El plano interno de Helmholtz (IHP)
Es el plano imaginario que pasa por los centros de los iones específicamente adsorbidos, a una distancia de la superficie del electrodo. La densidad de carga total de estos iones se denota como .
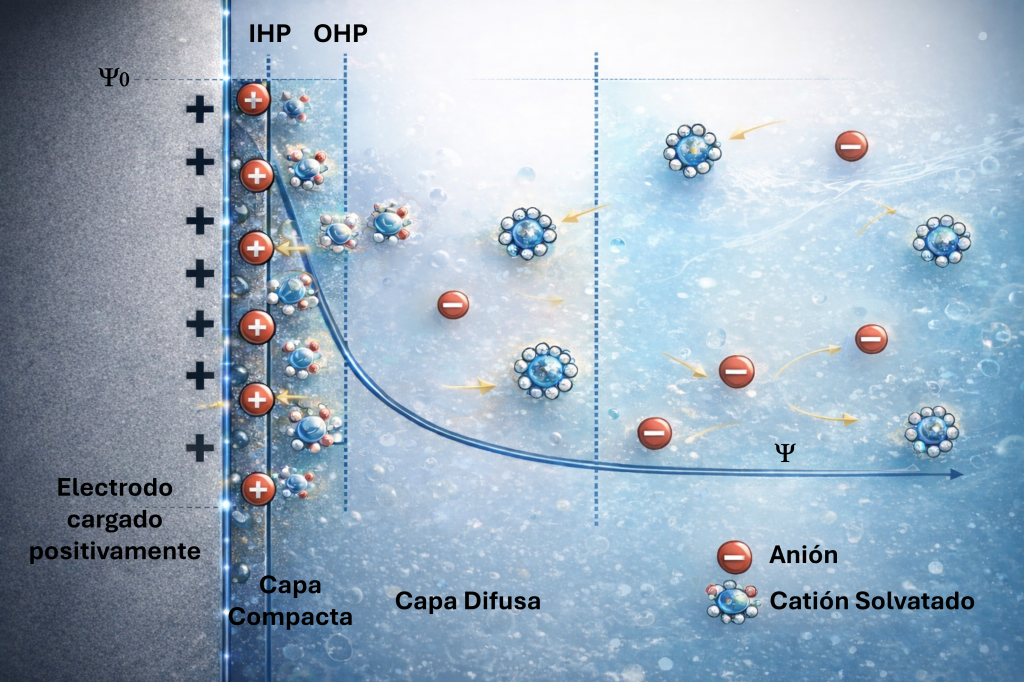
El plano externo de Helmholtz (OHP)
Los iones que conservan su envoltura de moléculas de disolvente (iones solvatados) no pueden acercarse al metal más allá de una distancia , determinada por el radio de la esfera de solvatación. El plano que pasa por los centros de los iones solvatados más próximos es el OHP. Estos iones interactúan con el electrodo únicamente mediante fuerzas electrostáticas de largo alcance: no importa de qué ion se trate, solo importa su carga. Se dice que están adsorbidos de forma no específica.
La capa difusa
Más allá del OHP, la agitación térmica impide que los iones formen una capa ordenada. En su lugar se distribuyen en una región tridimensional (la capa difusa) cuyo grosor depende de la concentración iónica de la solución. A concentraciones superiores a 10⁻² M, por ejemplo, el grueso de la capa difusa es inferior a ~10 nm; a concentraciones bajas puede extenderse hasta centenares de nanómetros.
El balance de cargas total en el lado de la solución se expresa:
donde es la densidad de carga en la capa difusa. Esta ecuación no es trivial: dice que el sistema ajusta las contribuciones relativas de adsorción específica y distribución difusa para compensar exactamente la carga del metal, en todo momento y a todo potencial.
Por qué la doble capa afecta a las reacciones reales
Una especie electroactiva que quiere reaccionar en el electrodo tiene que llegar hasta su superficie. Si no está específicamente adsorbida, lo más cerca que puede aproximarse es al OHP. El potencial que experimenta en ese punto no es el potencial aplicado al electrodo: es menor en una cantidad igual a la caída de potencial a través de la capa difusa, .
En la práctica, esto significa que la velocidad de una reacción electroquímica puede depender de la concentración de electrolito de fondo, de la naturaleza del disolvente y de la adsorción de especies inertes (todo ello a través de su efecto sobre la estructura de la doble capa) incluso cuando ninguna de esas variables participa directamente en la reacción química. Este efecto, conocido como efecto Frumkin, es una fuente habitual de artefactos en la interpretación de datos cinéticos electroquímicos.
Además, en experimentos con concentraciones muy bajas de especie electroactiva, la corriente no faradaica necesaria para cargar la doble capa puede ser comparable o superior a la corriente faradaica de la reacción de interés. Distinguir ambas contribuciones y diseñar experimentos donde la corriente faradaica pueda extraerse con fiabilidad es un problema de ingeniería experimental que no tiene solución trivial.
Dónde aparece la doble capa en la tecnología real: ejemplos
Supercondensadores
Los supercondensadores (también llamados ultracondensadores o EDLC, electric double-layer capacitors) almacenan energía exclusivamente en la doble capa, sin reacciones faradaicas. Eso les permite ciclos de carga y descarga ultrarrápidos y vidas útiles de millones de ciclos, a cambio de una densidad de energía menor que la de las baterías. El diseño de su electrodo, típicamente carbón activado con áreas superficiales de 1000–3000 m²/g, es un ejercicio de maximización de .
Galvanizado y protección contra la corrosión
La morfología de un depósito metálico (liso, granular, dendrítico) depende en gran medida de qué especies se adsorben específicamente en la capa interna de Helmholtz durante el proceso. Los aditivos de baños galvánicos, tales como brillantadores, niveladores, funcionan exactamente modulando esa adsorción.
Baterías y pilas de combustible
En cualquier interfaz electrodo/electrolito de una batería, los iones deben navegar a través de la capa difusa y la capa interna antes de participar en la reacción de intercalación o transferencia de carga. La resistencia de la interfaz, es decir, la formación de la SEI (solid electrolyte interphase) en baterías de litio, o la cinética del ORR (oxygen reduction reaction) en pilas de combustible, son fenómenos donde la estructura de la doble capa tiene un papel directo y medible.
Lo que aquí has leído es solo una simplificación de unas pocas páginas de Electrochemical Methods de Bard y Faulkner, un texto que, con razón, se considera la “biblia” de la electroquímica moderna.