La tabla periódica tiene más de cien elementos, pero solo uno de ellos domina hoy el almacenamiento de energía portátil y la electrificación del transporte: el litio. ¿Pero por qué? Como veremos en este artículo, no es por una moda tecnológica, sino por su física, química y termodinámica, y entenderlo requiere volver a la interfaz electrodo-electrolito que vimos en el artículo anterior sobre la doble capa eléctrica.
El litio es el metal más ligero y uno de los más reactivos. Esa combinación permite altas densidades energéticas: más energía almacenada en menos masa y volumen. Además, su potencial electroquímico extremadamente bajo favorece baterías de alto voltaje, recargables y con buen rendimiento a lo largo de muchos ciclos. Sin embargo, hace falta remarcar que el litio es también un metal escaso en términos absolutos y geopolíticamente concentrado en unos pocos países. Otros metales tales como el sodio y el magnesio (alternativas más abundantes) se siguen investigando como sustitutos, pero como veremos, hasta hoy ninguno iguala su rendimiento dentro de las restricciones que impone la física del sistema.
Que un material con ese perfil se haya convertido en el núcleo de la transición energética obliga a preguntarse: ¿qué tiene el litio que no tiene ningún otro?
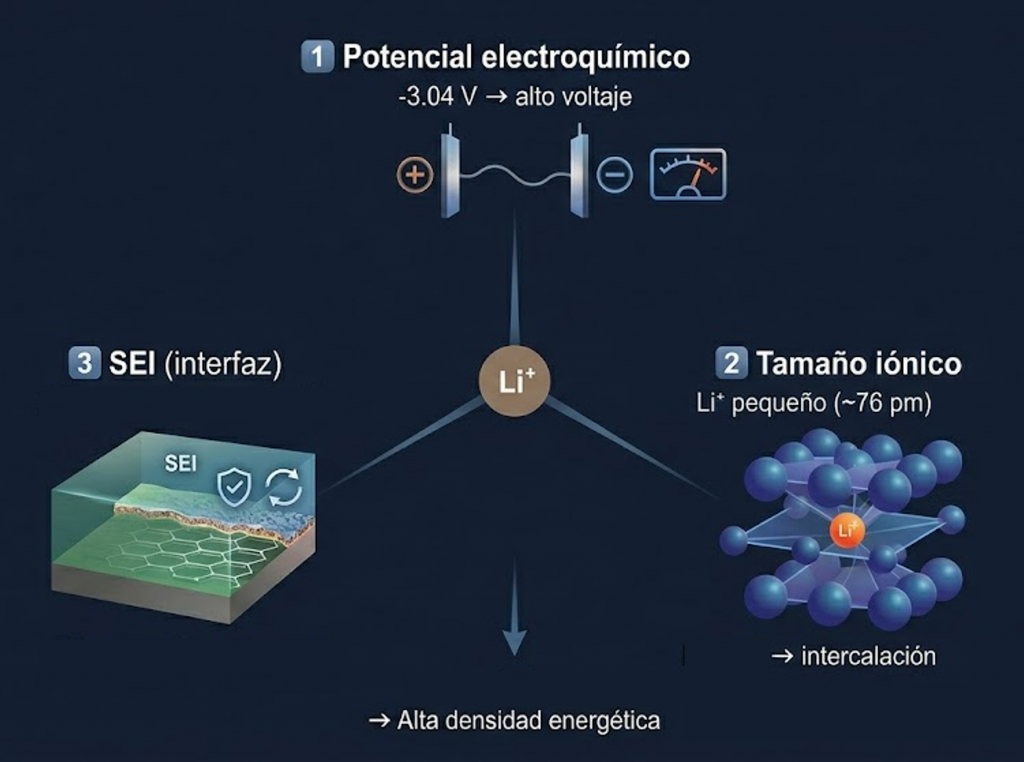
1) El potencial electroquímico
Una de las razones principales por las que el litio se usa en las baterías es su potencial electroquímicoDefiniciónEl potencial electroquímico (µ) es una magnitud termodinámica que cuantifica la energía potencial total de una especie química cargada (como un ion o un electrón) en una fase determinada. Combina la energía debida a la composición química (potencial químico) y la energía debida al campo eléctrico local. muy bajo, es decir, muy negativo. En una batería, el voltaje depende de la diferencia de potencial entre sus dos electrodos: cuanto más negativo es el electrodo negativo, mayor puede ser el voltaje de la celda y, por tanto, mayor la energía que la batería puede entregar por cada ion que se mueve. Este metal tiene un potencial estándar de reducción de −3.04 V frente al electrodo estándar de hidrógeno, mientras que el sodio está en −2.71 V. Esa diferencia, aunque parezca pequeña, es importante en la práctica porque ayuda a conseguir baterías con mayor voltaje y mejor densidad de energía; además, es mucho más ligero que otros metales alcalinos, lo que refuerza su ventaja en baterías de alta energía. Por eso, las baterías de ión litio suelen trabajar en torno a 3.6–3.7 V, frente a valores más bajos en muchas baterías de ión sodio, normalmente alrededor de 3.0–3.3 V.1
2) El radio iónico
La segunda gran razón por la que el litio se usa en baterías es su radio iónico. El ion Li⁺ es muy pequeño, con un radio de aproximadamente 76 pm, lo que facilita que entre y salga de materiales sólidos con poca distorsión de la red cristalina. Esa propiedad es clave en las baterías de ión litio, porque permite que el litio se intercale2 de forma reversible en materiales como LiCoO₂ o LiFePO₄ durante la carga y la descarga, sin colapsar la estructura del electrodo en condiciones normales de operación. De hecho, este mecanismo de intercalación fue esencial en el desarrollo de la batería de ión litio reconocida con el Nobel de Química de 2019. Además, al ser un ion tan pequeño, Li⁺ también presenta una alta densidad de carga, lo que influye en su interacción con el electrolito y en el comportamiento de la interfaz electrodo-electrolito, un factor importante para la cinética y la estabilidad del dispositivo. 3
3) SEI: la interfaz sólido-electrolito
Aquí aparece una de las ideas más contraintuitivas de la batería de ión litio: el electrolito orgánico no es realmente estable en contacto con un ánodo de litio metálico o con grafito muy litiado, porque el potencial del ánodo es tan bajo que el electrolito tiende a reducirse. En lugar de provocar una degradación continua e incontrolada, esa descomposición inicial forma una película sólida muy fina llamada SEIDefiniciónLa Solid Electrolyte Interphase (SEI) es una capa de pasivación heterogénea que se forma en la superficie de los electrodos de una batería (principalmente en el ánodo de grafito) durante los primeros ciclos de carga y descarga. Esta capa es el resultado de la descomposición irreversible del electrolito líquido al entrar en contacto con el potencial electroquímico del electrodo. (solid electrolyte interphase), o interfaz sólido-electrolito. Una SEI bien formada es la clave del funcionamiento: deja pasar iones Li⁺, pero bloquea el paso de electrones, de modo que la reducción del electrolito se frena y la reacción se autolimita.4
La SEI no es una capa uniforme ni estática, sino una película heterogénea compuesta por productos de descomposición del electrolito, como carbonatos, fluoruros, óxidos y sales de litio, con un espesor del orden de nanómetros. Su composición y estabilidad dependen del electrolito, del material del ánodo, de la temperatura y del protocolo de formación y carga, y por eso es uno de los factores más importantes en la vida útil de la batería. En condiciones ideales, la SEI protege el ánodo; en condiciones reales, sin embargo, puede seguir creciendo lentamente, consumir litio activo y aumentar la resistencia interna, lo que contribuye a la pérdida de capacidad con el envejecimiento.5
Baterías: litio vs. sodio
Frente al litio, el sodio tiene una ventaja clara: es mucho más abundante que el litio y su distribución geológica es más uniforme, lo que lo convierte en una opción muy atractiva para almacenamiento estacionario y aplicaciones donde el coste de la materia prima importa más que la máxima densidad de energía. Sin embargo, desde el punto de vista electroquímico y de materiales, el sodio parte con desventajas importantes. El ion Na⁺ es más grande que el Li⁺, y ese mayor tamaño dificulta su intercalación en muchas estructuras cristalinas diseñadas originalmente para litio, obligando a usar materiales distintos, como ciertos óxidos en capas, compuestos tipo NASICONDefiniciónNASICON es el acrónimo de Sodium (Na) Super Ionic Conductor. Se refiere a una familia de sólidos cristalinos que presentan una conductividad iónica excepcionalmente alta, comparable a la de los electrolitos líquidos, pero en estado sólido. Su estructura es el estándar para el desarrollo de baterías de estado sólido y sensores de sodio. Su fórmula general es Na_(1+x)Zr_(2)Si_(x)P_(3-x)O_(12), 0< x < 3 y es el equivalente en sodio al LISICON (Lithium Super Ionic Conductor) o cátodos de azul de Prusia.6,7
En el ánodo ocurre algo parecido: el grafito, que funciona tan bien en baterías de ión litio, no intercala sodio de manera eficiente en condiciones normales. Por eso, muchas baterías de ión sodio recurren a hard carbon, una forma de carbono más desordenada que puede alojar Na⁺, pero con un rendimiento energético generalmente inferior al del grafito en litio. El resultado es que las baterías de ión sodio suelen ofrecer menor densidad de energía y, en muchas formulaciones actuales, un voltaje medio más bajo que sus equivalentes de ión litio.6,7
Esto no significa que el sodio sea una mala opción. Al contrario: para almacenamiento en red, respaldo renovable y aplicaciones estacionarias, su abundancia, menor coste potencial y buena seguridad pueden compensar parte de su menor rendimiento gravimétrico. Pero precisamente por eso el litio sigue dominando en vehículos eléctricos, electrónica portátil y usos donde peso, volumen y autonomía son críticos.
El coste oculto del litio: geografía y riesgos geopolíticos
Todo lo anterior explica por qué el litio ganó la competencia química. Pero esa victoria tiene un coste que no aparece en ninguna ecuación electroquímica: su cadena de suministro es extremadamente vulnerable.
Con concentraciones de ~20 ppm en la corteza terrestre, el litio no es raro en términos absolutos, pero sus depósitos explotables económicamente están distribuidos de forma muy desigual. El Triángulo del Litio (Argentina, Bolivia, Chile) concentra más del 50-60% de las reservas mundiales conocidas, principalmente en salares como Uyuni, Atacama y Hombre Muerto. Australia domina la producción de espodumena (hard rock), mientras China controla ~65-75% de la capacidad global de refinación y procesamiento químico.
Esta dependencia crea riesgos estructurales:
- Interrupciones geopolíticas (tensiones EE.UU.-China, disputas en el Triángulo del Litio)
- Volatilidad de precios ligada a la concentración geográfica
- Cuellos de botella en refinación (China domina el paso crítico entre mineral y material de batería)
No es posible entender la supremacía técnica del litio sin considerar su vulnerabilidad estratégica. Los artículos de la colección «Metales de la electrificación« de Raw Science exploran esta cadena en detalle: desde dónde viene el litio, cómo se procesa, qué países controlan cada etapa, y qué significaría reemplazarlo por alternativas como sodio.
En resumen
El Dominio del Litio en Baterías
Haz clic en cada pilar para explorar la física y química detrás de su éxito.
⚡ Potencial Electroquímico Extremadamente Bajo
El litio tiene un potencial estándar de reducción de -3.04 V (frente a los -2.71 V del sodio). Al ser el electrodo negativo tan bajo, la diferencia de potencial con el cátodo es mayor. Resultado: Baterías de mayor voltaje (3.6-3.7 V) y mucha más energía entregada por cada ion que se mueve.
🔬 Un Radio Iónico Diminuto (76 pm)
El tamaño del ion Li⁺ es ideal para la intercalación reversible. Entra y sale de las estructuras sólidas de los electrodos (como el grafito o el LiCoO₂) sin colapsar ni distorsionar gravemente la red cristalina. El sodio (Na⁺), al ser más grande, obliga a usar materiales distintos y menos eficientes energéticamente.
🛡️ La Magia de la SEI (Solid Electrolyte Interphase)
El electrolito se descompone al contacto con el ánodo, pero en lugar de degradar la batería, forma una película protectora a escala nanométrica. Una SEI bien formada deja pasar los iones Li⁺, pero bloquea los electrones, deteniendo la reacción y garantizando la vida útil de la batería a lo largo de miles de ciclos.
⚖️ Litio vs. Sodio
- Litio: Mayor densidad energética y voltaje. Rey indiscutible del vehículo eléctrico y dispositivos portátiles.
- Sodio: Menor rendimiento, pero mucho más abundante, barato y uniforme. Ideal para almacenamiento estacionario (red eléctrica).
🌍 Vulnerabilidad Geopolítica
- Extracción: Concentrada en el Triángulo del Litio (Argentina, Bolivia, Chile) y Australia.
- Refinación: China controla entre el 65% y el 75% del procesamiento químico global, creando cuellos de botella y riesgos estructurales.
Referencias
- M.M. Hasan, et al. (2025) Advancing energy storage: The future trajectory of lithium-ion battery technologies, Journal of Energy Storage, 120,116511. doi: 10.1016/j.est.2025.116511.
- Kuhn. A. et al. (2022) Lithium Intercalation Mechanism and Critical Role of Structural Water in Layered H2V3O8 High-Capacity Cathode Material for Lithium-Ion Batteries, Chemistry of Materials, 34, 2, 694-705. doi: 10.1021/acs.chemmater.1c03283
- Zhang, H. et al. (2024) Enhanced Li-ion intercalation kinetics and lattice oxygen stability in single-crystalline Ni-rich Co-poor layered cathodes. J. Mater. Chem. A, 12 (6) 3682-3688. doi: 10.1039/D3TA07156A
- Aktekin, B., et al. (2023) SEI growth on Lithium metal anodes in solid-state batteries quantified with coulometric titration time analysis. Nat Commun 14, 6946. doi: 10.1038/s41467-023-42512-y
- Tao, L. et al. (2025) Revealing the roles of the solid–electrolyte interphase in designing stable, fast-charging, low-temperature Li-ion batteries, Proc. Natl. Acad. Sci. U.S.A. 122 (13) e2420398122. doi: 10.1073/pnas.2420398122.
- Prajapati, A.K. et al.(2024) A review on anode materials for lithium/sodium-ion batteries, Journal of Energy Chemistry, 83, 509-540. doi: 10.1016/j.jechem.2023.04.043.
- Rehm, M. et al. (2025) Comparing the electrical performance of commercial sodium-ion and lithium-iron-phosphate batteries, Journal of Power Sources, 633, 236290. doi: 10.1016/j.jpowsour.2025.236290.